
O roli farmaceuty w obrocie środkami kontrolowanymi i cyfryzacji usług w hurtowni farmaceutycznej
Rozmowa z mgr farm. Jolantą Pabijanek - Osobą odpowiedzialną za obrót środkami odurzającymi i substancjami psychotropowymi w hurtowni farmaceutycznej Urtica.
Zarządzanie środkami kontrolowanymi w farmacji to zadanie wymagające niezwykłej precyzji, dogłębnej znajomości przepisów prawnych, ale także umiejętności zarządzania skomplikowanymi procesami logistycznymi oraz dokumentacją. To wszystko w celu zapewnienia bezpieczeństwa i zdrowia pacjentom. Aby dowiedzieć się więcej o tym, jak wygląda praca w tym obszarze oraz jak cyfryzacja zmienia codzienną praktykę, rozmawiamy z mgr farm. Jolantą Pabijanek – osobą odpowiedzialną za obrót środkami odurzającymi i substancjami psychotropowymi w hurtowni farmaceutycznej. Ekspertka podzieli się z nami swoimi doświadczeniami i refleksjami na temat wyzwań, które wiążą się z jej rolą.
Jolu, jakie są Twoje zadania w Dziale Jakości Urtica?
Zadania, jakie czekają na mnie w ramach funkcjonowania Działu Jakości, wynikają bezpośrednio ze stanowiska jakie piastuję – jestem osobą odpowiedzialną za obrót środkami odurzającymi i substancjami psychotropowymi. Zakres moich obowiązków i zadań został opisany w Ustawie o przeciwdziałaniu narkomanii z 29 lipca 2005 roku w artykule 40. oraz późniejszych rozporządzeniach ministra zdrowia.
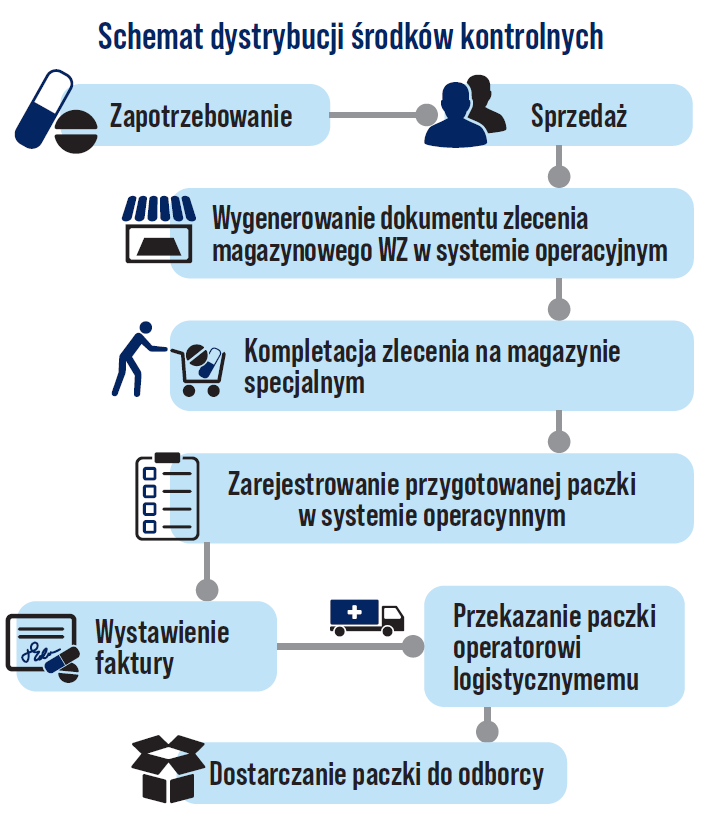
Chcąc w skrócie opisać moje obowiązki: jestem odpowiedzialna za stworzenie systemu nadzorującego prawidłowy obrót hurtowy środkami kontrolowanymi od chwili, w której zamawiamy towar do naszych magazynów, do momentu dostarczenia paczki ze środkami kontrolowanymi do naszego odbiorcy.
Urtica zawsze stara się wychodzić naprzeciw oczekiwaniom klientów, jednakże do kwestii formalnych przywiązujemy szczególną wagę. Powiedz, dlaczego z punktu widzenia osoby odpowiedzialnej za obrót środkami odurzającymi i substancjami psychotropowym zachowanie zasad jest tak istotne?
Środki kontrolowane są szczególnym rodzajem leków. Prawo opisuje w precyzyjny sposób warunki prowadzenia hurtowej dystrybucji: od wymogów, jakie musi spełnić pomieszczenie, w którym są one przechowywane, poprzez prowadzenie ewidencji przychodów i rozchodów, kwalifikację naszych kontrahentów, przekazywanie do utylizacji, po specyficzne wymogi, jakie towarzyszą sprzedaży tych środków.
Mając na uwadze oczekiwania naszych klientów oraz dbając o wysoką jakość usług, jakie świadczymy, przywiązujemy ogromną wagę do zgodności naszych działań z obowiązującymi przepisami prawa, szczególnie w tym obszarze asortymentowym.
W związku z obowiązującymi wymogami pomieszczenie służące do przechowywania środków kontrolowanych jest zabezpieczone przed dostępem osób nieupoważnionych alarmem, objęte systemem kontroli dostępu, wyposażone w monitoring. Kontrola stanów magazynowych odbywa się tam codziennie. Zespół pracowników magazynu specjalnego to mała grupa doświadczonych, dobrze zorganizowanych osób, rozumiejąca swoje obowiązki i zadania, co przekłada się na zadowolenie odbiorców z jakości naszej usługi.

Znając specyfikę pracy farmaceutów działu jakości hurtowni farmaceutycznej, na pewno masz do czynienia z prowadzeniem dokumentacji jakościowej. Jak to wygląda z perspektywy osoby odpowiedzialnej za obrót środkami kontrolowanymi?
Jest dokładnie tak, jak mówisz. Dużą grupę czynności należących do moich obowiązków jest prowadzenie dokumentacji. Jest to przede wszystkim określona przepisami ewidencja przychodów i rozchodów, obejmująca wszystkie grupy środków kontrolowanych. W naszej hurtowni posiadamy obecnie system ewidencjonowania obrotu w postaci Elektronicznej książki narkotycznej.
Warto wspomnieć również o kwalifikacji środków kontrolowanych do utylizacji. Zajmuję się przygotowywaniem i przesyłaniem do Wojewódzkiego Inspektoratu Farmaceutycznego (WIF) zawiadomień dotyczących zniszczenia środków kontrolowanych. Następnie muszę skompletować dokumentację z samego procesu utylizacji.
Ważne miejsce zajmują również czynności związane z procesem reklamacyjnym, który z natury jest trudny, a gdy dotyczy środków kontrolowanych, szczególnie. Staramy się spełniać oczekiwania naszych odbiorców, niestety nie jest możliwe wyeliminowanie wszystkich błędów w całym procesie dystrybucji. W mechanizmie reklamacyjnym sprawuję bezpośredni nadzór, gromadzę stosowną dokumentację umożliwiającą weryfikację zgłoszonych reklamacji i podejmuję decyzję odnośnie do zasadności zgłoszenia. Zbędne ruchy na stanach magazynowych w obrębie tego asortymentu powinny być zminimalizowane, aby nie budzić żadnych niejasnych skojarzeń. Pamiętajmy o obowiązującym hurtownie farmaceutyczne raportowaniu transakcji w Zintegrowanym Systemie Monitorowania Obrotu Produktami Leczniczymi (ZSMOPL) i Krajowej Organizacji Weryfikacji Autentyczności Leków (KOWAL).
Wszystkie opisane elementy mojej pracy są dość szczegółowo uregulowanie prawnie i opisane w Prawie farmaceutycznym, Dobrej Praktyce Dystrybucyjnej (DPD) oraz Ustawie o przeciwdziałaniu narkomanii i towarzyszącym im rozporządzeniom.
W ciągu ostatnich lat uwidacznia sią dążenie do cyfryzacji kolejnych procesów. Urtica także proponuje nowe rozwiązania swoim klientom, takie jak SWAL czy e-Urtica. Jak myślisz, czy rynek farmaceutyczny jest gotowy na takie zmiany?
Farmacja zawsze chłonęła nowości z rynku informatycznego. Była to chyba pierwsza z gałęzi ochrony zdrowia, która została szybko i sprawnie zinformatyzowana. Mam tu na myśli programy apteczne wspomagające pracę farmaceuty w aptece. Tak jak wspomniałaś, Urtica również uruchomiła swoją platformę współpracy online dla swoich klientów. Jeśli chodzi o mój obszar, platforma ta pozwala na elektroniczne potwierdzanie, przesyłanie i archiwizację zapotrzebowań, które zgodnie z Rozporządzeniem Ministra Zdrowia z dnia 20 października 2015 roku poz. 1819 par. 5 zamawiający przedkłada u dostawcy. Platforma nakłada na użytkownika konieczność posiadania kwalifikowanego podpisu elektronicznego, ale korzyści płynące z możliwości korzystania ze scyfryzowanej obsługi w kwestii związanej z obowiązkiem dostarczenia zapotrzebowania do dostawcy są niebagatelne. Klienci mogą w ten sposób zredukować swoje koszty, chociażby w postaci oszczędności na papierze.
Interpretacja przepisów wydana przez Główny Inspektorat Farmaceutyczny (GIF) w lutym 2023 (źródło – Komunikat GIF w sprawie dopuszczalnej formy zapotrzebowań na nabycie środków odurzających i substancji psychotropowych) nie pozostawia wątpliwości i wyraźnie nakreśla kierunek zmian i oczekiwań urzędu.
Jolu, bardzo dziękuję za rozmowę. Twoja praca jest niezwykle odpowiedzialna i wymaga dużej siły charakteru. Na co dzień stoisz na straży norm i przepisów, co musi być bardzo stresujące. Jak sobie z tym radzisz?
W zawód farmaceuty wpisana jest odpowiedzialność i odwaga w podejmowaniu decyzji, bez względu gdzie ten zawód jest wykonywany. Moje stanowisko jest dość niszowe, a związane z nim obowiązki mocno obwarowane różnymi wymogami prawnymi, mimo to staram się im wszystkim sprostać. Bardzo pomaga mi w tym atmosfera panująca w Urtice. Dział Jakości (zespół, do którego bezpośrednio należę) oraz Dział Reklamacji (z którym ściśle współpracuję) to grupa wspaniałych, ciekawych i ciepłych ludzi, dzięki którym można przenosić góry i dokonywać niemożliwego. To buduje i pozwala pokonać wszelkie trudności.
Rozmawiała Aleksandra Cencora
Piśmiennictwo
-
Rozporządzenie Ministra Zdrowia z dnia 7 lipca 2016 r. w sprawie wydawania zezwoleń na obrót hurtowy środkami odurzającymi, substancjami psychotropowymi lub prekursorami kategorii 1.
-
Rozporządzenie Ministra Zdrowia z dnia 20 lutego 2024 r. w sprawie szczegółowych warunków i trybu postępowania ze środkami odurzającymi, substancjami psychotropowymi i prekursorami kategorii 1, ich mieszaninami lub odpadami oraz produktami leczniczymi, zepsutymi, sfałszowanymi lub którym upłynął termin ważności, zawierającymi w swoim składzie środki odurzające, substancje psychotropowe lub prekursory kategorii 1.
-
Rozporządzenie Ministra Zdrowia z dnia 11 września 2006 r. w sprawie środków odurzających, substancji psychotropowych, prekursorów kategorii 1 i preparatów zawierających te środki lub substancje.
-
Komunikat GIF w sprawie dopuszczalnej formy zapotrzebowań na nabycie środków odurzających i substancji psychotropowych – Główny Inspektorat Farmaceutyczny – Portal Gov.pl (www.gov.pl).
-
Ustawa z dnia 6 września 2001 r. Prawo farmaceutyczne.
-
ROZPORZĄDZENIE MINISTRA ZDROWIA z dnia 13 marca 2015 r. w sprawie wymagań Dobrej Praktyki Dystrybucyjnej.
Powyższy artykuł został opublikowany na łamach 62. wydania kwartalnika „Farmakoekonomiki Szpitalnej", którego jesteśmy wydawcą. Czasopismo jest skierowane do pracowników farmacji szpitalnej.
Przypominamy, że czasopismo można otrzymać w formie bezpłatnej prenumeraty.
DOŁĄCZ DO GRONA PRENUMERATORÓW!